
始于19世纪初的手术治疗,经过不断发展,实现了“治愈”一小部分患者的目标;
始于19世纪末的放射治疗,发展到上世纪50年代,单独或联合的作用使得约1/3患者治愈;
始于20世纪初的化疗,又进一步提高了肿瘤的治疗效果。
三种传统治疗方法走向极致,但远未达到人们期望的治疗目标。
肿瘤的免疫治疗虽发展晚,却以前所未有的速度进入临床,并有望最终成为治愈肿瘤的重要武器。目前的免疫治疗策略包括针对肿瘤细胞或免疫调节分子的单克隆抗体,基于细胞的疗法,例如离体活化T细胞和天然杀伤(NK)细胞的过继转移,以及癌症疫苗。在参与免疫应答的免疫细胞中,树突细胞是目前已知的功能最强的抗原提呈细胞,相当于免疫抗癌大军的司令塔。
1973年,加拿大科学家拉尔夫斯坦曼在小鼠脾脏中发现了一种特殊的细胞,因其细胞膜伸出许多类似于神经细胞的树突故而得名。随后,他一直在研究这种细胞在人体抵抗病原体中发挥的重要性,以及它如何被用来治疗疾病。34年后,他不幸被诊断为最为难治,预后极差的胰腺癌。于是他基于树突状细胞设计了一系列癌症治疗方案。包括三种树突细胞疫苗,最终研发出一种疫苗,使用斯坦曼的肿瘤表面特异性多肽刺激斯坦曼自己的树突状细胞,然后用激活的树突状细胞启动免疫应答。当这些树突状细胞注射回体内时,已经可以识别并攻击肿瘤细胞了。像他这样的胰腺癌患者存活时间一般是几周到几个月。最终,“拉尔夫坚信他的树突状细胞延长了自己的生命。
2011年10月3号,斯坦曼因其研究成果共同分享了诺贝尔生理及医学奖,但他永远不会知道这个消息了。在68岁这一年,与癌症斗争了4年半之后,他在诺贝尔奖揭晓的3天前病逝。

树突状细胞(Dendritic Cells,DC):是一群异质性的细胞, 抗原提呈功能最强, 是唯一能够激活初始型T细胞的专职抗原递呈细胞。
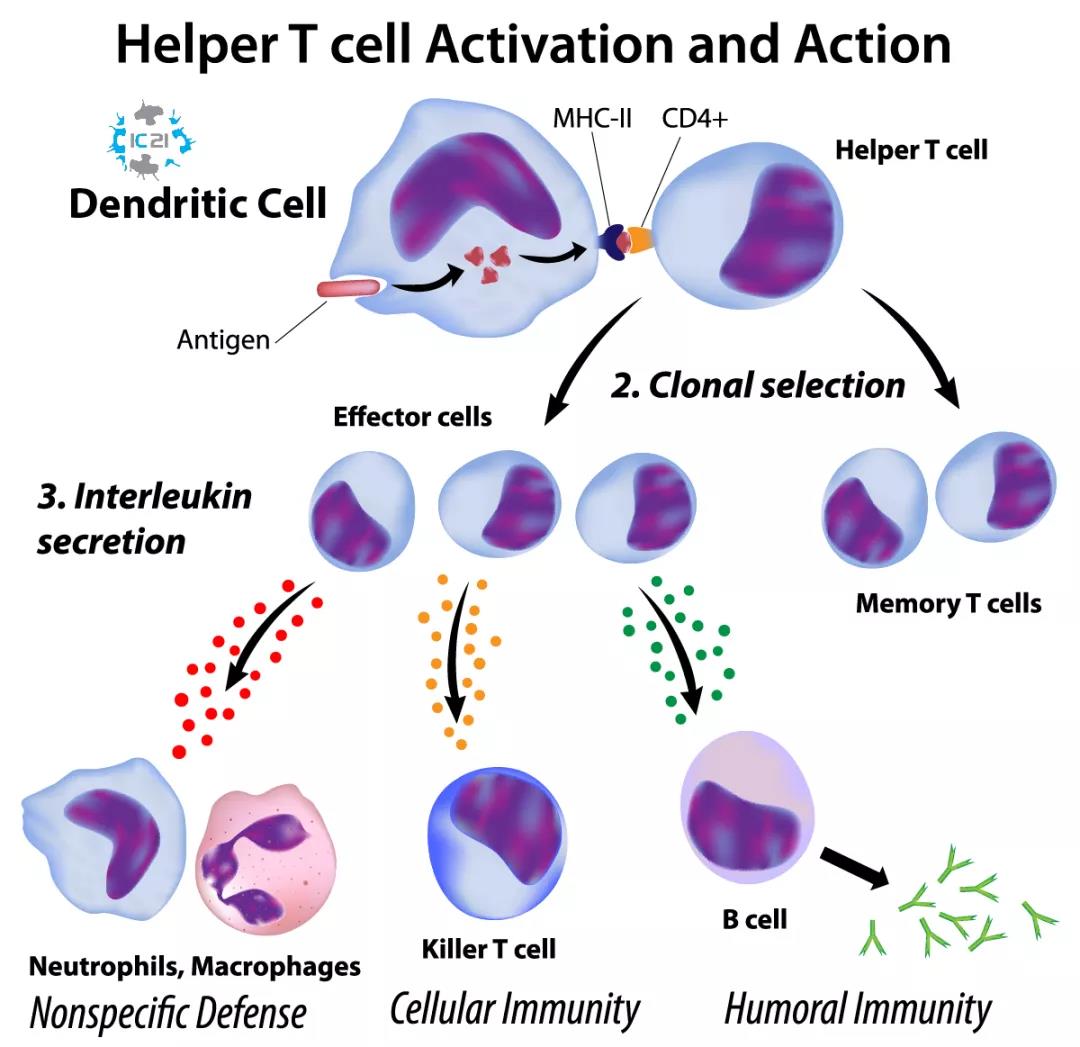

正常人体内也会产生突变细胞进一步变为癌细胞。由于我们有免疫系统的保护,通常我们不会得癌症。
癌细胞表面的肽由称为MHC或HLA的分子递呈,这些呈递在细胞上的肽是独特的,我们称为特异性抗原,
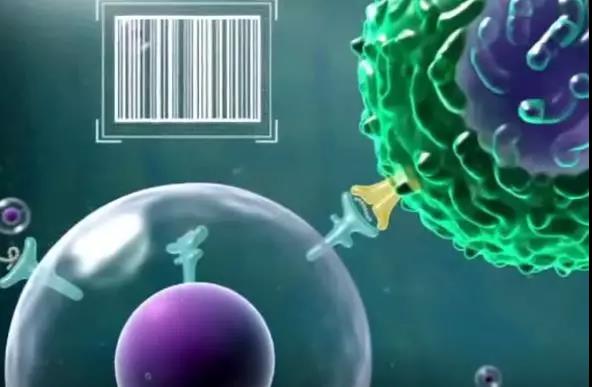
体内的肿瘤细胞信息在循环过程中,会被体内的巡逻兵树突细胞识别,癌细胞由树突状细胞吸收并分解,并在细胞表面上作出标记,树突细胞同时把癌细胞的特征也就是癌抗原“告诉”(呈递)数以百亿的杀手T细胞,杀手T细胞通过T细胞受体(TCR 像条形码扫描机)连续扫描这些细胞的表面,T细胞的扫描功能就是所谓的免疫监视。如果T细胞识别这些肽是异常的,就会发起攻击。
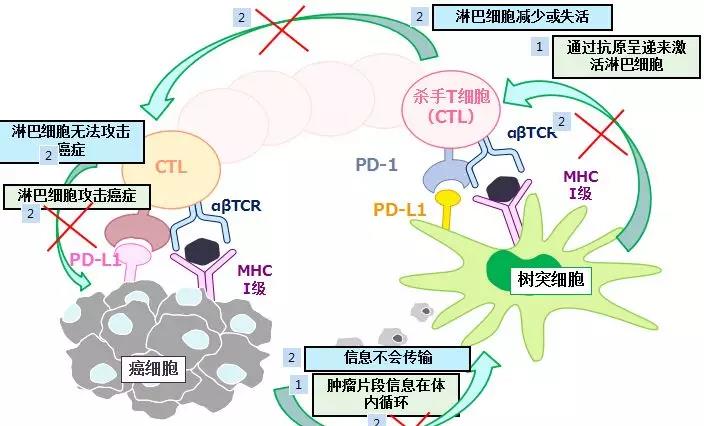
癌症的发生好比是癌细胞与免疫系统在身体里面的一场大战,最后免疫系统战败,癌细胞一统天下,在身体里任意生长,诱发癌症。免疫系统战败的原因有很多,归根结底有两个:
1、癌细胞伪装得好,使得树突细胞无法识别和杀灭癌细胞;
2、体内免疫细胞数量下降,没有足够的兵力(杀手T细胞)去消灭癌细胞。
因此,如何让树突细胞重新识别癌细胞是医学研究的重点。

人体的免疫系统中本来就有这种树突状细胞,但数量和活力都不够围歼癌变细胞的程度。有潜力成为树突状细胞的前体细胞可以通过一个特定的方法从血液中分离出来。借助于某种特定的信使,在试管中分离出来的细胞可以获得免疫能力。当前体细胞成熟为树突状细胞时,他们即可捕获特定的蛋白质(例如肿瘤抗原)。
由于树突状细胞抗肿瘤特性与疫苗原理一致,因此树突细胞疗法在临床中更多的被称为树突细胞疫苗。
目前树突状细 胞肿瘤疫苗正在被迅速、广泛的研究 ,并且已在动物实验和 早期的临床实验中取得了很有意义的结果。这些研究结果表 明: 树突状细胞肿瘤疫苗不仅能够诱发针对原发肿瘤的免疫 应答 , 而且也 能够诱发针对 转移肿瘤的免疫应答 , 并且 CD4 + 、 CD8 + T 淋巴 细胞 和自 然杀 伤细 胞 ( natur e kille r cells, N Ks)都参与抗肿瘤免疫应答。
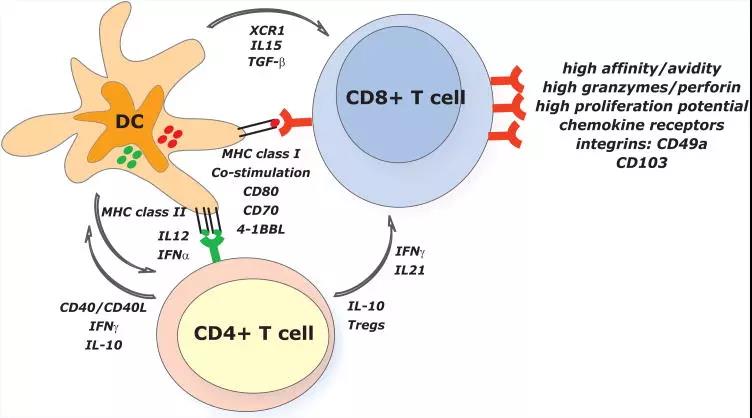
树突细胞可通过各种方式用于癌症疫苗接种,包括:
1)体内树突细胞捕获的非靶向肽/蛋白和基于核酸的疫苗
2)直接与抗树突抗体偶联的抗原组成的疫苗,
3 )由体外产生的负载抗原的树突组成的疫苗。

机体各种常见的病毒感染性疾病和肿瘤的发生与机体DC功能的缺失或缺陷有直接关系,所以恢复体内特异性DC功能成为治疗和预防这类疾病的关键。T-DC由于特异性的优势抗原表位肽的使用,使被激活的T细胞具有特异性和靶向性,通过修复、恢复和增强患者自身细胞免疫功能,打破了机体免疫全身和局部的耐受状态,从而实现全身和局部机体免疫的重建。
研究证明,T-DC主要以以动员体内各种细胞因子为主要手段来清除靶目标,这使得重建的免疫系统在清除靶目标的同时大大降低了对正常细胞损伤作用。
体外重建的DC在回输体内时可以激活静息T细胞产生初次免疫应答的细胞,激活的T细胞可以被点状放大并进一步增殖。一个树突能激活100~3000 个T细胞。大部分效应T细胞发挥清除病毒的作用,另一部分会存活长达十几年到几十年成为记忆性T细胞,在下一次接触到低剂量抗原就可发生高强度的免疫应答。所以,基于T-DC修复和重建的免疫防护系统可以持续发挥作用数十年,并在适当的条件下可以重新进入循环发挥作用。

临床中正在开展许多针对癌症的治疗性疫苗接种途径。在国际临床试验官网clinicaltrials.gov中搜索术语树突细胞疫苗,有54个临床研究。这些研究中的一个共同特征是疫苗接种的关键步骤是将癌抗原有效呈递给T细胞(图2)。因为DC是最有效的抗原呈递细胞,因此,利用它们的多样性可能产生改进的治疗性疫苗。
树突细胞疫苗在各个癌症中取得了令人振奋的研究数据,全球肿瘤医生网医学部查阅了大量文献,为大家挑选了一些具有重磅数据,并且有望上市的研究,希望给患者多一份希望和战胜癌症的信心!
一项正在H. Lee Moffitt癌症中心和研究所进行的HER-2脉冲DC1疫苗试验将测试在高风险HER-2高表达和中度表达乳腺癌中的安全性和免疫原性,用来预防乳腺癌的复发。
研究人员认为结合化疗的树突状细胞疫苗可以增加完全反应,使乳腺癌特异性免疫细胞有更大的机会发挥功能,并预防乳腺癌的复发。入组患者在初始诱导疫苗后,进行免疫分析,随后每隔3个月施用三剂加强疫苗,并分别进行免疫分析。
2019年第50届妇科肿瘤学会(SGO)年会上,一项二期临床试验SOV02(NCT02107950)最终结果公布:对复发,铂敏感,上皮卵巢癌患者使用基于树突状细胞的免疫疗法DCVAC / OvCA添加到标准卡铂和吉西他滨方案,可以使晚期复发的卵巢癌患者总生存期(OS)延长一年多,这个数据绝对称得上惊艳!
▶DCVAC / OvCa将卵巢癌二线治疗的死亡风险降低了62%。
▶总生存期(OS)显着增加13.4个月。中位数无进展生存率(mPFS)增加了1.8个月。
▶即将开展全球三期研究。
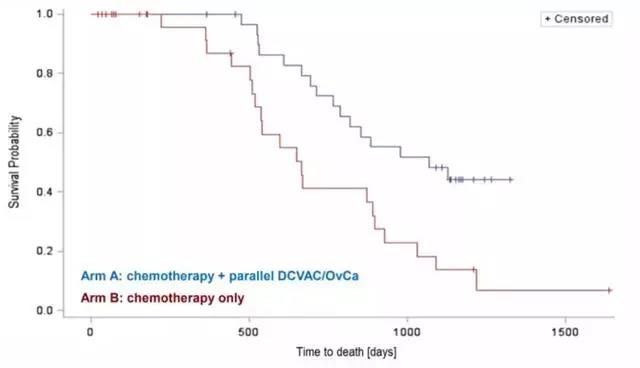
最近的是卵巢癌的三期树突细胞疫苗(DCVAC / OvCA)试验,将于今年下半年开始。一旦开始招募,全球肿瘤医生网医学部将第一时间为大家公布。
加州大学洛杉矶分校的科学家已经发现了一种树突状细胞疫苗,其扩大了免疫系统对非小细胞肺癌(NSCLC)的反应,这是最常见的肺癌形式。该研究是第一个在人类中测试疫苗的研究,具有重要的临床意义,因为非小细胞肺癌和其他晚期癌症患者是非常难以成功治疗的,该方法可以提高目前抗PD-1免疫治疗对癌症的杀伤力。
该研究在线发表在美国癌症研究协会同行评议的临床癌症研究杂志《Clinical Cancer Research》上。
在I期临床试验中,将CCL21-树突疫苗直接施用于16例非小细胞肺癌患者的肿瘤中,两次剂量间隔约7天。加州大学洛杉矶分校的科学家们在接种疫苗当天比较了每个患者的一组肿瘤样本。
结果显示,在第56天,25%的患者病情稳定(意味着其肿瘤的大小不增加或减少)。在54%的患者中,CD8细胞浸润于肿瘤中,在接种疫苗后患者的PD-L1表达也显着增加。副作用是可控的,主要限于流感样症状,恶心和疲劳。
一项新的小型新研究表明,一种直接注射到单个肿瘤中的新型癌症“疫苗”可以激活免疫系统 攻击全身的癌细胞。
这项研究是由纽约西奈山伊坎医学院淋巴瘤免疫治疗项目主任Joshua Brody博士领导的,他说,“将疫苗注射到一个肿瘤后(原位疫苗接种),我们看到整个身体内的肿瘤消失”。
这项重磅的研究4月8日发表在国际顶级期刊“ Nature medicine”杂志上。
在抗癌疫苗的治疗下,11名患者中有8名取得了病情缓解,其中完全缓解的患者有2名。1名达到完全缓解的患者,无进展生存期已经接近4年!这些积极结果,也让研究人员们充满信心,现在该治疗方法也正在乳腺癌和头颈癌患者中进行检测。
生物科技公司Northwest Biotherapeutics近期公布了其先导疗法DCVax®-L治疗新诊多形性胶质母细胞瘤(GBM)的III期临床研究的中期试验数据。
该研究共有331例患者入组,最后一批患者入组时间为在2015年11月。所有患者在入组研究前已接受手术切除并接受了6周标准护理治疗SOC)放化疗。研究中,患者以2:1的比例被随机分配接受SOC+DCVax-L(n=232)或SOC+安慰剂(n=99)。【注:该研究将外周血单核细胞(PBMC)用作安慰剂】
截止到论文发表时,入组临床超过三年的患者中,67例(30%)存活超过30个月,44例(24.2%)存活超过36个月。预计这些患者的中位生存期为46.5至88.2个月。在分析时,参加试验的331名患者中有108名(32.6%)仍然保持存活。
值得注意的是,每一个激活的、装载肿瘤特异性抗原的树突状细胞都具有很大的乘数效应(multiplier effect),可动员数百个T细胞和其他免疫细胞。因此,小剂量的此类树突状细胞就可以动员大规模、持久的免疫应答。同样重要的是,DCVax-L是无毒的。在迄今为止的临床研究中,长达10多年和超过1000个疗程的治疗中没有出现任何诸如化疗涉及的毒性,也没有发生治疗相关的严重不良事件。

如今,全球细胞免疫治疗技术日新月异,研发领域不断突破,技术优化升级,加速为人类疾病带来新的治疗手段。尤其是美国,德国,日本等医疗水平发达的国家,对树突细胞的研发及临床应用走在世界前列。
我国目前批准的细胞免疫治疗的临床试验项目不多,DC细胞疗法的价值、安全性和潜力还有待挖掘。相信一旦整体政策完备推出,将带动我国相关临床治疗的操作规范和标准执行,为我国肿瘤患者治疗增添新选择。
2010年4月29日,FDA批准了首个癌症治疗疫苗PROVENGE(sipuleucel T)用于晚期前列腺癌的治疗,使该药成为第一个在美国被批准用于治疗的树突细胞疗法,开创了癌症免疫治疗的新时代,这项批复标志着20年的不懈努力终于取得成功。

德国癌症治疗专家Frank Gansauge教授,带队研发的LANEX-DC是一种利用肿瘤抗原对患者自体树突(DC)细胞进行特异性免疫刺激培养,以DC细胞为基础的肿瘤疫苗技术。通过采集患者血液,分离、筛选出高纯度DC细胞,混合了细胞因子GM-CSF、肿瘤特异性抗原(PAP)等物质进行培育,使DC细胞活化,再回输患者,激活患者体内的T淋巴细胞,从而产生针对大量表达PAP的肿瘤细胞的特异性免疫杀伤效应,消灭癌细胞!临床已证实对人类已知的恶性肿瘤,如肺癌、肝癌、肾癌、乳腺癌、皮肤癌等多种肿瘤有效。详情点击:德国树突细胞疫苗治疗原理介绍
这种树突细胞免疫治疗方案在其他国家不是没有,但是收效甚微,目前在国内的顶级医科大学研发的产品其活性因子的生存期只有21天,也就意味着21天内就要进行下一个疗程。而LDG团队的LANEX-DC治疗法采用高度提纯的树突细胞,一个疗程可以维持6个月,更重要的是他们把病患的复发率从50%降低到7%。同时细胞活性因子从培养室到植入患者体内,之间的存活时间可以持续8个小时,目前国内医科大学制备后基本存活时间就在20分钟之内。 技术上存在巨大差距。
目前,日本的免疫治疗技术已经更新至第五代,即个性化的精准复合细胞免疫疗法。
通过对患者的癌组织进行免疫组织化学染色,以及流式细胞定量检测分析,全面了解患者体内PD-1、NK、杀伤性T细胞等免疫细胞水平,从而掌握体内的免疫功能及反应情况,在此基础上,根据患者的个体化病情选择αβ T细胞疗法、树突细胞疫苗疗法、NK细胞疗法、 γΔT细胞疗法等组合,相当于个性化定制。价格约在22-26万人民币。
融合细胞疗法是世界领先的癌症研究中心哈佛大学Dana-farber癌症研究所与东京慈惠医科大学共同开发,是最具前瞻性的癌症免疫治疗。利用患者自身的癌细胞来攻击癌细胞,确立了至今为止全新的癌症治疗方法。价格约35万人民币。详情点击:日本新一代融合细胞疗法横空出世,精准狙击癌细胞!
这是一种很理想的疗法,我们都知道癌症形成的原因之一,就是癌细胞隐藏的很好,树突细胞无法识别癌细胞,大家想象一下,把自己的癌细胞和树突细胞融合,形成携带多种癌细胞表面的特异性抗原的树突细胞,这些树突细胞就具备了识别肿瘤细胞的能力,我们把这些细胞回输导体内,他就会教导体细胞去识别不同的癌抗原的癌细胞,一组去找a抗原,一组去找b抗原癌细胞,把他们统统消灭,同时结合增强体内T细胞的辅助治疗白细胞介素12一起使用,能够有效增加杀手T细胞的数量,从而达到最佳的抗癌效果。目前在国际上被广泛研究。
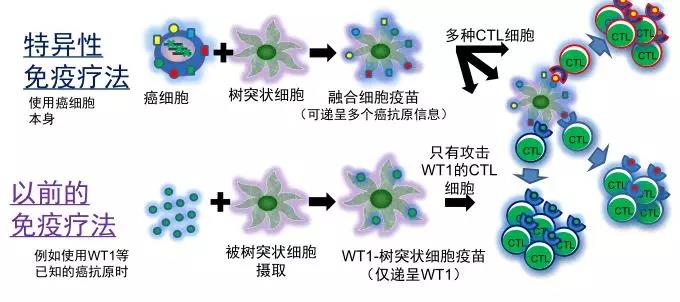
简单来说,就是
1.利用患者自身的癌细胞,与患者自身的树突细胞进行体外融合。
2.得到能够表达所有癌抗原的新树突细胞,制备成个体化的融合细胞疫苗。
3.将融合细胞回输入患者体内识别癌细胞。


肿瘤手术前保质较差, 术后恢复慢, 且害怕隐匿性瘤细胞没有被彻底根除的患者
需要注意的是 , 细胞免疫疗法对于晚期癌症意者肿瘤的缩小效果不明显, 针对晚期癌症的患者在保持生活品质的同时有延长寿命的效果;作为术后的辅助治疗法可以问制复发, 治疗效果可维持较长时间;与化疗、靶向药、 PD1抑制剂等真古疗法联合治疗,效果会更佳。
主要适用于实体肿瘤:头颈部肿瘤、食道癌、肺癌、胃癌、乳腺癌、肝癌、膜腺癌、结亘肠癌、卵巢癌、子宫癌、彗癌、前列腺癌、恶性黑色素瘤、肉瘤、部分恶性淋芭瘤。
