2025上半年,21款重磅抗癌药在国内获批上市!覆盖十大癌症
小编 2025-07-02
2025年上半年,21种重磅抗癌新药在国内获批上市!覆盖十大癌种
肺癌、肝癌、乳腺癌等又有新药啦!2025上半年,国内21款抗癌疗法获批上市并有望进入今年的医保目录,还有多款疗法将在下半年上市!更大的好消息是,有些已经在中国开展临床试验,这意味着国内的患者可以有机会同步接受美国最新抗癌药物的治疗,并且是免费的。想参加的患者可提交资料至医学部申请评估。
据统计,十年前,一种新药从开始申请到最终被中国患者吃到平均需要5年时间,这指的是自费药。如果再算上纳入医保目录所需时间,平均需要等6~8年。相信很多病友对2018年的一部电影《我不是药神》感同身受,也让全社会深刻认识到我们国家癌症病友们面临的生存绝境--无药可用!很多病友在苦苦等待中绝望离去。。。
值得振奋的是,我们国家再也不是过去那个医疗远远落后美国的国家!近两年,众多癌症已经打破了治疗僵局,迎来了首款靶向药物,又有很多幸运的病友们等来了新的希望和治疗选择,相信未来会越来越好!
肺癌新药
01、EGFR20ins-埃万妥单抗
无进展生存期翻倍!埃万妥单抗在华获批上市!
药品信息
药品名称:锐珂®(埃万妥单抗注射液)
研发公司:西安杨森
药物介绍:2025年2月,锐珂®(埃万妥单抗注射液)在中国正式获批上市,用于经检测确认携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗!这是一种新型的EGFR-MET双特异性抗体,靶向激活和耐药的EGFR和MET突变和扩增。2021 年 5 月基于 I 期研究(CHRYSALIS)的积极结果获 FDA 加速批准,是全球首款也是唯一一款获批上市的 EGFR/cMET 双抗。
上市时间:2025年2月
02、EGFR--芦沙妥珠单抗
首款国研TROP2 ADC震撼上市!EGFR肺癌迎来曙光
药品信息
药品名称:芦康沙妥珠单抗(SKB264 商品名:佳泰莱)
研发公司:四川科伦博泰
药物介绍:芦康沙妥珠单抗(SKB264 商品名:佳泰莱)是由中国科伦博泰生物享誉国际的ADC研发平台—OptiDC研发的具有代表性的靶向TROP2的创新ADC。TROP2是一种广泛分布于多种上皮肿瘤表面的跨膜糖蛋白,具有与抗TROP2抗体特异性相互结合的能力。在非小细胞肺癌(NSCLC)中,TROP2的阳性表达率高达89%因此,TROP2被视为治疗NSCLC的一个极具潜力的靶点。
2025年3月10日,国研创新药物芦康沙妥珠单抗(SKB264/Sac-TMT)上市,用于治疗经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)和含铂化疗治疗失败的局部晚期或转移性 EGFR突变非小细胞肺癌(NSCLC)成人患者。这意味着芦康沙妥珠单抗成为EGFR-TKI耐药后治疗的新选择!更值得一提的是,这是首款中国原创的用于肺癌的TROP2新型抗体偶联药物(ADC),为肺癌的精准治疗开启全新的纪元!
上市时间:2025年3月
03、EGFR/ALK-欧狄沃单抗
药品信息
药品名称:欧狄沃单抗
研发公司:百时美施贵宝
药物介绍:4月22日,百时美施贵宝刚刚宣布,PD-1抑制剂欧狄沃(纳武利尤单抗注射液)获得中国NMPA批准新增适应症:联合含铂化疗作为新辅助治疗,术后继续以欧狄沃作为单药辅助治疗,用于治疗可手术切除的II、 IIIA和IIIB期且无已知表皮生长因子受体(EGFR)突变或间变性淋巴瘤激酶(ALK)重排的成人非小细胞肺癌(NSCLC) 患者。
上市时间:2025年4月
04、EGFR--利厄替尼药
品信息
药物名称:利厄替尼片
研发公司:奥赛康药业
药物介绍:4月25日,奥赛康药业申报的1类新药利厄替尼片的新适应症上市申请获得批准。利厄替尼是具有全新分子结构的第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),本次为该产品获批的第二项适应症。根据奥赛康药业此前公告,该药本次获批的定适应症为:具有EGFR外显子19缺失(19DEL)或外显子21置换突变(L858R)的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗。
上市时间:2025年4月
05、PD-L1--依沃西单抗
药品信息
药物名称:依沃西单抗
研发公司:康方生物
药物介绍:4月25日,中国国家药监局(NMPA)官网最新公示,康方生物PD-1/VEGF双抗依沃西的新适应症上市申请已获得批准。根据中国国家药监局药品审评中心(CDE)优先审评公示信息可知,该药本次获批的适应症为:单药用于PD-L1阳性[肿瘤比例评分(TPS)≥1%]的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌(NSCLC)的一线治疗。
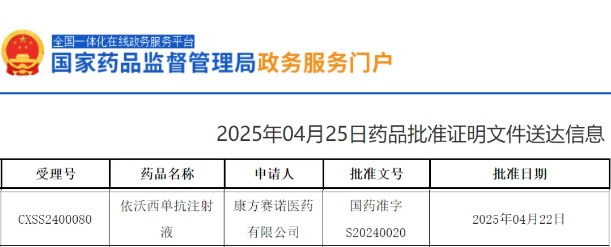
上市时间:2025年4月
06、EGFR--阿美替尼
药品信息
药物名称:阿美替尼
研发公司:江苏豪森药业
药物介绍:阿美替尼是一款三代EGFR-TKI。2020年3月,该产品获批用于
既往经EGFR-TKI治疗进展,且T790M突变阳性的局部晚期或转移性NSCLC患者;2021年12月,该产品获批一线治疗具有EGFR外显子19缺失或外显子21(L858R)置换突变阳性的局部晚期或转移性NSCLC成人患者;2024年3月,该产品获批用于含铂根治性放化疗后未出现疾病进展的不可切除的局部晚期EGFR外显子19缺失或外显子21(L858R)置换突变的NSCLC患者治疗。
5月9日,中国国家药监局(NMPA)官网刚刚发布的批件信息显示,翰森制药三代EGFR-TKI甲磺酸阿美替尼片的新适应症上市申请获得批准。根据翰森制药此前新闻稿介绍,该药本次获批的适应症为:用于具有表皮生长因素受体(EGFR)外显子19缺失或外显子21(L858R)置换突变阳性的非小细胞肺癌(NSCLC)成人患者肿瘤切除术后的辅助治疗。这也是阿美替尼在中国获批的第四项适应症。
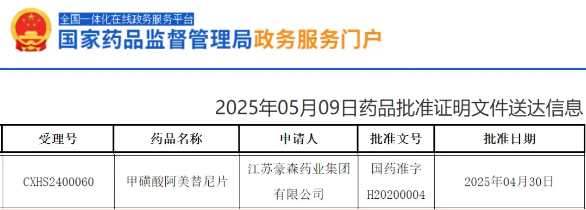
上市时间:2025年5月
7、HER2--瑞康曲妥珠单抗
药品信息药物名称:瑞康曲妥珠单抗
研发公司:恒瑞医药
药物介绍:瑞康曲妥珠单抗是一款靶向 HER2 的抗体偶联药物(ADC),由曲妥珠单抗、可裂解连接子及拓扑异构酶 I 抑制剂有效载荷 SHR169265 巧妙组合而成。5月29日,注射用瑞康曲妥珠单抗正式获批上市。适应症为:单药适用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
上市时间:2025年5月
8、KRAS--戈来雷塞片
药品信息
药名名称:戈来雷塞片(glecirasib,JAB-21822)
研发公司:加科思
药品介绍:JAB-21822是加科思自主研发的KRAS G12C抑制剂。临床前研究数据表明,其可单独使用,治疗含KRAS G12C突变的实体瘤,同时在KRAS G12C抑制剂治疗发生耐药后,联合SHP2抑制剂有望有效克服和逆转KRAS抑制剂的耐药问题。2025年5月22日,针对KRAS突变有效,革命性国研抗癌药--枸橼酸戈来雷塞片(glecirasib,JAB-21822)获得中国国家药品监督管理局药品审评中心(NMPA)批准正式上市,用于单药治疗至少接受过一种系统性治疗的KRAS G12C突变型晚期非小细胞肺癌(NSCLC)成人患者。同时,这款药物也有了自己的响当当的大名--艾瑞凯!
上市时间:2025年5月
09、MET--赛沃替尼
药品信息
药名名称:沃瑞沙(ORPATHYS,赛沃替尼/ savolitinib)
研发公司:和黄医药
药品介绍:6月30日,和黄医药宣布沃瑞沙(ORPATHYS,赛沃替尼/ savolitinib)和泰瑞沙(TAGRISSO,奥希替尼/ osimertinib)的联合疗法的新药上市申请获中国国家药品监督管理局(NMPA)批准,用于治疗表皮生长因子受体(EGFR)基因突变阳性经EGFR酪氨酸激酶抑制剂(TKI)治疗后进展的伴MET扩增的局部晚期或转移性非鳞状非小细胞肺癌患者。沃瑞沙是一款选择性MET抑制剂,用于治疗伴有MET外显子14 跳变的局部晚期或转移性非小细胞肺癌成人患者。临床研究结果显示:沃瑞沙和泰瑞沙的联合疗法降低患者的疾病进展风险达66%,中位PFS为8.2个月,而化疗组则为4.5个月。
上市时间:2025年6月30日
10、小细胞肺癌--度伐利尤单抗
药品信息
药名名称:度伐利尤单抗
研发公司:阿斯利康
药品介绍:6月4日,阿斯利康宣布抗PD-L1单抗度伐利尤单抗已获中国国家药品监督管理局(NMPA)批准新适应症,作为单药用于在接受铂类药物为基础的放化疗后未出现疾病进展的局限期小细胞肺癌(LS-SCLC)成人患者的治疗。此次获批是基于ADRIATIC 3期临床试验的积极结果,数据显示:接受度伐利尤单抗治疗的患者显示出了显著的总生存获益,三年总生存率高达57%,度伐利尤单抗有望成为中国乃至全球的治疗新标准。
上市时间:2025年6月4日
乳腺癌新药
01、PIK3CA--伊那利塞片
药品信息
药名名称:伊那利塞片
研发公司:罗氏
药品介绍:2025年3月11日,抗癌圈再次传来一个好消息,中国国家药品监督管理局(NMPA)批准了伊那利塞片的上市申请,该药与哌柏西利+氟维司群联合,用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后出现复发)、PIK3CA突变、HR(激素受体)阳性、HER2(人表皮生长因子受体2)阴性的局部晚期或转移性乳腺癌成人患者的治疗。
值得一提的是,伊那利塞片是中国首个获批的第三代高选择性PI3Kα抑制剂,填补了HR+/HER2-晚期乳腺癌精准治疗的空白。同时,也是首个获得中美双重突破性疗法认证的HR+乳腺癌治疗产品,具有里程碑氏的重要意义!国内首款!第三代高选择性PI3Kα抑制剂-伊那利塞片在华获批,填补晚期乳腺癌无药可用困境!
上市时间:2025年3月11日
胃癌新药
01、HER2--泽尼达妥单抗
药品信息
药名名称:泽尼达妥单抗(ZW25)
研发公司:百济神州
药品介绍:5月29日,中国国家药监局(NMPA)官网最新公示,百济神州申报的1类新药注射用泽尼达妥单抗上市申请已经获得批准,适用于既往接受过全身治疗的HER2高表达(IHC3+)的不可切除局部晚期或转移性胆道癌患者。泽尼达妥单抗(ZW25)是一种双特异性抗体,可诱导抗肿瘤活性,并且对HER2阳性经过各种治疗失败的患者具有良好的耐受性。
上市时间:2025年5月29日
肝癌新药
01、纳武利尤单抗注射液+伊匹木单抗注射液
药品信息
药名名称:纳武利尤单抗注射液+伊匹木单抗注射液
研发公司:百时美施贵宝
药品介绍:2025年3月31日,百时美施贵宝公司研发的两款肿瘤免疫治疗药物——纳武利尤单抗注射液+伊匹木单抗注射液的新适应证,获得中国国家药品监督管理局(NMPA)批准,用于不可切除或晚期肝细胞癌(HCC) 成人患者的一线治疗。
上市时间:2025年3月31日
卵巢癌新药
01、塞纳帕利
药品信息
药名名称:塞纳帕利
研发公司:英派药业
药品介绍:1月16日,英派药业宣布其自主研发的塞纳帕利胶囊已获得NMPA批准上市,用于晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗。塞纳帕利是由英派药业自主研发的新型、高效的PARP1/2抑制剂,具有独特的分子结构,使其具备体外和体内高活性,以及高靶向选择性和广泛的安全窗口。华东医药拥有塞纳帕利在中国大陆的独家市场推广权益。
上市时间:2025年1月16日
尿路上皮癌新药
01、厄达替尼
药品信息
药名名称:厄达替尼片
研发公司:强生
药品介绍:1月13日,强生(Johnson & Johnson)宣布口服泛FGFR酪氨酸激酶抑制剂厄达替尼片(erdafitinib)的上市申请已获NMPA批准,用于治疗携带易感型FGFR3基因变异,且既往接受至少一线含抗PD-1或抗PD-L1期间或之后出现疾病进的手术不可切除的局部晚期或转移性尿路上皮癌(UC)成人患者。厄达替尼是一款新型靶向治疗药物,可显著改善携带FGFR3基因变异患者的总生存期和无进展生存期。3期临床试验(THOR)结果显示,对比化疗,在之前接受过PD-1或者PD-L1抑制剂治疗的患者中,厄达替尼改善了患者生存期,并降低死亡风险。
上市时间:2025年1月13日
鼻咽癌新药
01、派安普利单抗
药品信息
药名名称:派安普利单抗
研发公司:中国生物制药
药品介绍:2025年3月14日,抗PD-1单抗类药物-派安普利单抗注射液,新适应症上市申请也获得了中国国家药品监督管理局(NMPA)的批准,与化疗联合用于复发或转移鼻咽癌(NPC)的一线治疗。
上市时间:2025年3月14日
宫颈癌新药
01、卡瑞利珠单抗
药品信息
药名名称:卡瑞利珠单抗
研发公司:恒瑞
药品介绍:2025年5月21日,国家药监局(NMPA)官网传来重磅喜讯——恒瑞医药研发的“卡瑞利珠单抗”新适应证正式在中国获批!与“苹果酸法米替尼”联合,用于既往接受含铂化疗失败的复发或转移性宫颈癌的治疗!这也是该药在中国获批的第十个适应症!这一突破性进展,标志着国内妇科肿瘤免疫联合治疗领域再攀高峰!两款药物强强联手,以“免疫治疗+抗血管生成”双重机制精准打击肿瘤,有望打破复发转移困境,为晚期宫颈癌患者点燃生命新曙光!
上市时间:2025年5月21日
02、卡度尼利单抗
药品信息
药名名称:卡度尼利
研发公司:康方
药品介绍:6月4日,中国国家药监局(NMPA)官网最新公示,康方生物研发的PD-1/CTLA-4双特异性抗体卡度尼利单抗注射液的一项新适应症上市申请已获得批准。根据康方生物早先新闻稿,该药本次获批的适应症为:卡度尼利单抗加含铂化疗联合/不联合贝伐珠单抗用于一线治疗持续、复发或转移性宫颈癌。
上市时间:2025年6月4日
骨髓瘤新药
01、塔奎妥单抗
药品信息
药名名称:塔奎妥单抗(Talquetamab)
研发公司:强生
药品介绍:塔奎妥单抗(Talquetamab)是一种First-in-Class双特异性抗体和人源化单克隆抗体,同时也是一种CD3E调节剂,2025年2月11日,在我国获批用于成人复发或难治性多发性骨髓瘤的治疗。早在2023年8月9日,该药就已获得美国食品药品监督管理局(FDA)的加速批准,用于成人既往已接受过至少4种治疗(包括免疫调节剂、CD38单克隆抗体、蛋白酶体抑制剂抗)的复发性或难治性多发性骨髓瘤的治疗。
上市时间:2025年2月11日
02、埃纳妥单抗(elranatamab)
药品信息
药名名称:埃纳妥单抗(elranatamab)
研发公司:辉瑞
药品介绍:2025年3月10日,美国辉瑞公司(Pfizer)研发的双特异性抗体新药——埃纳妥单抗(elranatamab),获国家药品监督管理局(NMPA)附条件批准上市。该药主要用于既往接受过至少三线治疗(包括1种免疫调节剂、1种抗CD38单克隆抗体、1种蛋白酶体抑制剂)的复发或难治性多发性骨髓瘤(RRMM)成年患者的治疗。
上市时间:2025年3月10日
黑色素瘤新药
01、特瑞普利单抗
药品信息
药名名称:特瑞普利单抗
研发公司:君实
药品介绍:2025年4月25日),抗癌领域传来重磅好消息:君实生物自主研发的抗PD-1抗体——特瑞普利单抗获中国国家药品监督管理局(NMPA)批准(受理号:CXSS2400084/5),新增适应证为
不可切除或转移性黑色素瘤的一线治疗,它也成为了首个覆盖晚期黑色素瘤一线免疫治疗的国产PD-1单抗!
上市时间:2025年4月25日
以上新药仅为众多研发热点中的一小部分,还有众多的新药研发,创新技术纷纷在路上,相信2025年将有更多的药物获批上市!除此之外,还有多款正在研发的抗癌新药也显示出广谱抗癌的实力。“方舟援助计划”可以为患者提供上市新药和未上市新药免费治疗的机会。
相信随着医学研究的不断深入,越来越多的新药即将研发上市,将有更多的病友跨过一个又一个5年!
参考资料:美国FDA官网、中国NMPA官网












