生存期翻倍!全球首个实体瘤 CAR-T 疗法改写晚期胃癌生存记录
小编 2025-06-13
全球首个实体瘤CAR-T细胞疗法舒瑞基奥仑赛注射液(CT041、Satri-cel)治疗胃癌生存期翻倍
中位无进展生存期3.25vs1.77个月!全球首款实体瘤CAR-T疗法公布的最新研究数据振奋人心,有望改写晚期胃癌治疗格局!
胃癌在全球范围内是发病率和死亡率均位列第五的癌症,而中国是全球胃癌发病率最高的国家之一。大家谈胃癌“色变”的重要原因是胃癌的难治性,大部分患者在确诊时都为晚期,虽然近两年靶向及免疫治疗取得了重大突破,但无进展生存期也仅为6个月,总生存期在8-14个月左右,胃癌患者迫切需要更好的治疗方案。
值得振奋的是,2025年ASCO盛会上,中国研究人员公布了全球首个针对实体瘤特异性靶点Claudin18.2的CAR-T细胞疗法--CT041(舒瑞基奥仑赛注射液,Satri-cel)随机对照试验的卓越数据,证实了satri-cel治疗显著延长了既往接受过治疗的CLDN18.2阳性胃癌或胃食管交界处癌患者的无进展生存期,并显著提高了总生存期,且安全性可控,有望改写晚期胃癌生存记录!
生存期翻倍!全球首个实体瘤CAR-T疗法改写晚期胃癌生存记录
舒瑞基奥仑赛注射液是目前全球唯一一款在中国和美国获得临床试验许可(IND)的CLDN18.2CAR-T细胞治疗,有望成为全球首创产品!
2025年ASCO(美国临床肿瘤学会)年会上,舒瑞基奥仑赛治疗中国晚期胃/胃食管连接部癌(G/GEJC)的关键性II期临床试验(CT041-ST-01,NCT04581473)结果震撼公布,并发表于国际重磅期刊《柳叶刀》杂志上,引起巨大轰动!
这项在中国24个研究中心开展的开放标签、多中心、随机对照试验(RCT)旨在比较CAR-T疗法Satri-cel与标准治疗(SOC)在CLDN18.2阳性、至少两线既往治疗失败的晚期胃食管交界处(G/GEJC)患者中的疗效和安全性。
当患者对传统治疗耐药后,往往陷入无药可医的绝境。2022年3月22日至2024年7月29日期间,研究团队采用2:1随机分组,156例CLDN18.2阳性、至少两线治疗失败的患者被分为Satri-cel治疗组(104例)与标准治疗(TPC)组(52例)。Satri-cel组接受250×10⁶个细胞输注,最多3次;TPC组则由医生选择阿帕替尼、紫杉醇等常规药物治疗。值得关注的是,TPC组患者在病情进展或不耐受时,符合条件者可交叉接受Satri-cel治疗,这一设计更贴近真实临床场景。
数据截止至2024年10月18日的分析结果堪称震撼!
生存期显著延长
无进展生存期:9.07个月VS3.45个月。在ITT人群中,独立审查委员会评估的Satri-cel组中位无进展生存期为3.25个月,TPC组中位无进展生存期为1.77个月。疾病进展或死亡风险直降63%!
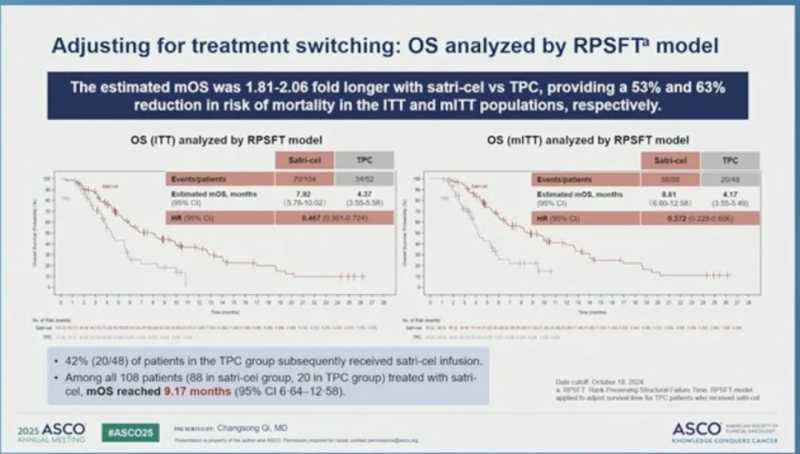
总生存期:14.42个月VS11.33个月。在ITT人群中,satri-cel组的中位总生存期为7.92个月,TPC组的中位总生存期为5.49个月。
更值得一提的是,汇总所有接受Satri-cel输注的108例患者,mOS达9.17个月,远超TPC(医生选择的治疗)组未接受该治疗患者的3.98个月,充分证实了Satri-cel的卓越疗效。
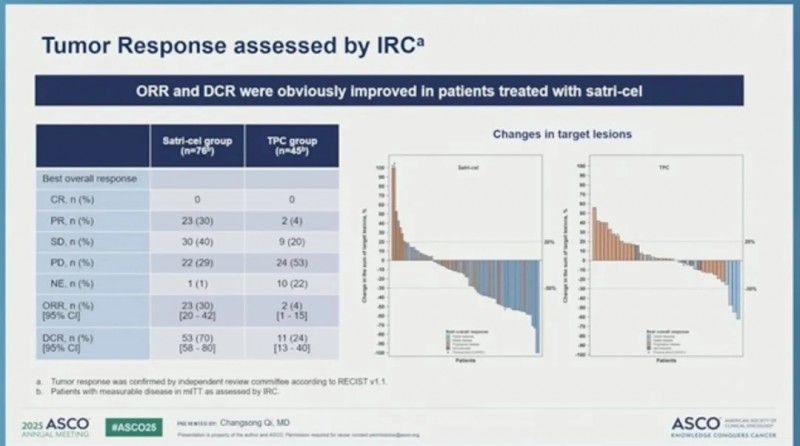
22%晚期胃癌肿瘤显著缩小
经独立审查委员会评估,satri-cel组确诊客观缓解率为22%(104名患者中23名),TPC组为4%(52名患者中2名);satri-cel组疾病控制率为63%(104名患者中65名),TPC组为25%(52名患者中13名)。
该研究的主要研究者、北京肿瘤医院沈琳教授表示:“CT041-ST-01试验是全球首个CAR-T细胞治疗实体瘤的随机对照临床研究。对于既往接受过大量治疗、治疗选择极其有限且预后不佳的晚期胃癌/胃食管交界处癌患者,satri-cel展现了突破性的疗效和显著的临床获益,包括显著提高的无进展生存期(PFS)、总生存期(OS)和肿瘤缓解率。这为那些无法通过其他疗法治愈的患者带来了新的希望。我们正在进一步探索satri-cel在辅助治疗和一线序贯治疗中的潜力,旨在更早地干预疾病进程,延长患者生存期,并最终寻求治愈方案。”
这项试验的成功,不仅为晚期G/GEJC癌患者点亮了生命之光,更标志着实体瘤细胞治疗时代的真正来临。随着Satri-cel加速迈向临床应用,我们有理由期待,未来将有更多癌症患者受益于这一创新疗法,见证生命奇迹的发生!
近日,全球首款Claudin18.2CAR-T舒瑞基奥仑赛注射液再次传来喜讯:中国国家药监局药品审评中心(CDE)官网最新公示-CT041自体CART细胞注射液拟纳入优先审批,适应症为既往接受过至少二线治疗失败的Claudin18.2(CLDN18.2)表达阳性的晚期胃/食管胃结合部(G/GEJ)腺癌。更好的消息是,这款CAR-T预计将于2025年上半年向国家药品监督管理局(NMPA)提交上市申请!这意味着,如果一切顺利,舒瑞基奥仑赛注射液(satri-cel)将成为全球首个上市的实体瘤CAR-T产品,造福中国及全球胃癌患

晚期胃癌获得完全缓解!中国CAR-T疗法造福全球患者
2020年7月,美国FDA正式批准了中国的CAR-T疗法CT041开展临床实验,这项1b期多中心开放标签研究(NCT04404595)正在美国6个地点开展临床试验,众多美国胃癌患者已成功入组。近期,美国两家知名的癌症中心分别报道了两位幸运的患者达到完全缓解和部分缓解,这意味着,中国CAR-T疗法正站在世界舞台绽放璀璨光芒,造福全球患者!
30岁年轻晚期印戒细胞胃癌患者CAR-T治疗后获得完全缓解
2019年12月,不到30岁的M先生确诊为晚期胃印戒细胞癌,膀胱顶和腹膜壁转移。在接受了4种全身毒性化疗方案以及多次细胞减灭手术联合腹腔热灌注化疗(HIPEC)后,病情仍在在不断进展。
2021年5月,M先生参加了CT-041CAR-T细胞疗法在美国进行的临床试验,第一次CAR-T细胞回输后,他可以吃一些固体食物,并在约5个月后首次进行直肠排便。第二次回输后仅4周,M先生的影像检查结果显示肿瘤靶病灶竟然全部消失,达到了完全缓解(CR),并且脾周结节和胃壁增厚完全消退,更让人无法相信的是,血液层面追踪体内残存细胞的ctDNA检测结果显示为阴性,这意味着M先生体内已经没有分子残留疾病(MRD)!而且第二次回输M先生没有皮疹,他的精力水平显著提高,使他能够独立照顾孩子。在第一次CT041输注后8个月,M先生持续处于完全缓解状态!这也是海外报道的首例Claudin18.2CAR-T治疗后达到完全缓解的胃癌患者!
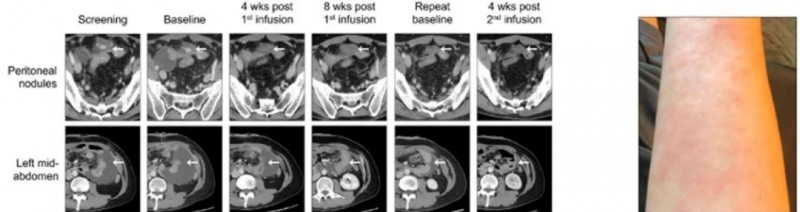
美国MD安德森公布治疗案例
全美癌症专科排名第一的MD安德森癌症中心在癌症免疫治疗学会(SITC)年会上公布了一例振奋人心的案例。
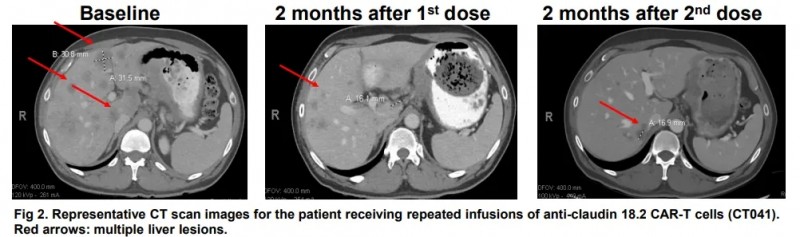
一名57岁男性的晚期胃癌(HER2阴性,PD-L1CPS10%)患者,肿瘤已经转移至肝脏,在接受5个周期的FOLFOX+Nivolumab方案和4个周期的FOLFIRI/Ramucirumab方案治疗后病情仍在不断进展。幸运的是,他在全美癌症专科排名第一MD安德森癌症进行了CLDN18.2的检测,显示为阳性,幸运的入组了全新的疗法--中国CAR-T的临床试验。
在预处理化疗后接受了第一次6亿个CT041细胞的治疗,影像显示肿瘤大小分别减小了19.2%、24.4%和26.9%。首次回输三个月后,患者接受了第二次6亿个CT041细胞的输注。CT扫描显示,与基线相比,肿瘤持续缩小,分别减小了34.6%(首次输注后4个月)和41.0%(首次输注后5个月)。
并且,这款CAR-T的安全性良好,截至目前,患者未报告发生严重不良事件,也未报告发生与胃肠道出血相关的不良事件(AE)。仅报告了短暂的3级或4级血液学毒性事件,其他所有AE均为1级或2级。
关于Satri-cel
Satri-cel是中国科济生物自主研发的一款针对Claudin18.2的自体CAR-T细胞候选产品,用于胃癌/胃食管交界处癌(GC/GEJ)和胰腺癌(PC)等Claudin18.2阳性实体瘤。
正在全球进行多项临床试验:
●研究者发起的试验(CT041-CG4006,NCT03874897);
●针对中国晚期GC/GEJ的确认性II期临床试验(CT041-ST-01,NCT04581473);
●针对中国PC辅助治疗的I期临床试验(CT041-ST-05,NCT05911217);
●针对北美晚期胃或胰腺腺癌的1b/2期临床试验(CT041-ST-02,NCT04404595)。
2022年1月,Satri-cel获得美国FDA授予的再生医学先进疗法(RMAT)资格,用于治疗Claudin18.2阳性晚期GC/GEJ癌,并于2021年11月获得EMA授予的PRIME资格,用于治疗晚期胃癌。2020年,Satri-cel获得美国FDA授予的孤儿药资格,用于治疗GC/GEJ,2021年获得EMA授予的孤儿药资格,用于治疗晚期胃癌。
目前,中国首创Claudin18.2CAR-T(Satri-cel)GC/GEJ关键II期临床试验患者入组也已经完成,我们期待这款卓越的疗法能够早日上市,造福更多的患者!
胃癌患者一定要检测的新兴靶点--Claudin18.2
Claudin18.2是一个泛肿瘤的靶点,在多种上皮肿瘤当中都有表达,尤其在胃癌和胰腺癌中存在较高的表达。在胃癌或胃食管结合部癌中,高达60%的患者检测到Claudin18.2的高度表达,成为近两年最具潜力的热门靶点,已有大量药物取得卓越的临床数据,为胃癌患者带来新曙光!
2024年6月25日,FDA批准zolbetuximab上市,联合含氟嘧啶和铂类化疗用于一线治疗治疗CLDN18.2阳性、不可切除、晚期或复发性胃癌或胃食管交界腺癌患者。这是第一个也是唯一一个靶向治疗患有CLDN18.2阳性这种毁灭性疾病的新选择!

除了上面获批的药物,还有更多的新药正在研发中,包括ADC药物、MET抑制剂、PD-1/PD-L1抑制剂等等,大家可以根据当前疾病的发展情况以及分子分型进行选择,也可联系医学部了解详细招募标准,进行入组评估。
M108
试验药组:LM302注射液
药物介绍:CLDN18.2ADCC单克隆抗体
适合患者:无法手术切除初治胃癌,需要CLDN18.2表达阳性。HER-2阴性的胃和胃食管结合部腺。
TQB2103
试验药组:TQB2103
药物介绍:Claudin18.2ADC
适合患者:标准治疗后不耐受或进展,需要CLDN18.2表达检测。HER-2阴性的胃和胃食管结合部腺癌。
相信上面这些在研药物给了晚期胃癌患者新的希望,同时也能看出,随着新型临床研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱,已经做了检测的病友可提交病历至医学部初步评估获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。
文献来源:
Claudin-18isoform2-specificCART-celltherapy(satri-cel)versustreatmentofphysician'schoiceforpreviouslytreatedadvancedgastricorgastro-oesophagealjunctioncancer(CT041-ST-01):arandomised,open-label,phase2trialQi,Changsongetal.












